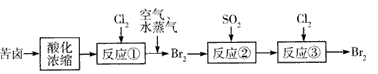
���_ľ�������ظ�ԭ���ی��衱֮�u������(n��i)������������и���������@Ӡ���}�V�YԴ����Һ�w�V����⛵V������������������V���������ȶ�N�V�a(ch��n)���ij�о��ԌW(xu��)��С�M�Mȡ�}�����u�ĝ�sҺ������K+��Mg2+�����Br-�����
SO42-��Cl-�ȣ���������ȡ�^�������Ȼ�⛾��w��Һ�壨Br2����������O(sh��)Ӌ����������
Ո����(j��)�������̣��ش����P(gu��n)���}��
��1�������۵����Q�ǣ�____________��������������Ҫ�IJ����x���У�_____________��
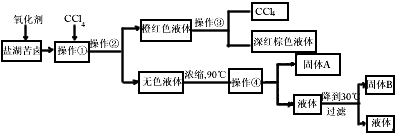
��2�������D�ܽ������������õ��^�����Ȼ�⛾��w������������ˮϴ��___________���x����w A�����wB������
��3��ͬ�W(xu��)�����һЩ�µķ������������������ں�oɫ��Һ�M�г��s�ἃ������䷽�����£�
�����P(gu��n)�Y�ϡ�
���O(sh��)Ӌ���s�^�̡�
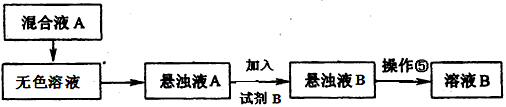
�����ڲ����ݽY(ji��)����l(f��)�F(xi��n)��ҺB���М�����������(y��ng)��ȡ�Ĵ�ʩ��__________________�����
�ڻ��ҺA����Ҫ�ɷ���__________________���������W(xu��)ʽ��
���z���s����
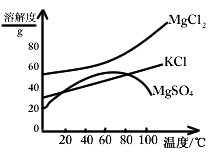
�۞�z�Mg2+��SO42-�Ƿ���M������ͨ���քeȡ�ҝ�ҺA�ό���Һ�ڃ�ԇ���С��M������
���Eһ���z�Mg2+�Ƿ���M���������һ֧ԇ���м���KOH��Һ������]�г���������������t����Mg2+�ѳ��M������
���E�����z�SO42-�Ƿ���M������һ֧ԇ���м���ij��Һ�������o�г�����������tSO42-�ѳ��M�����Ч����õ���_____________������ĸ������
A��Na2CO3 B��BaCl2 C��CaCl2
���@ȡ�����Ȼ�⛡�
�܌���ҺB�ӟᲢ����μ�l mol�� L-1���}����Һ����ͬ�r��pHԇ���z�y��Һ���ֱ��pH=5�rֹͣ���}�������õ���ҺC�����
����ҺC����________________����x�����Q���������ӟ����l(f��)���ò������������������ֱ�����F(xi��n)�^�ྦྷ�w��ʣ���^��ˮ�r�������ֹͣ�ӟ�����
�����}ӑՓ��
���M�в�����ǰ�����ȼӟ��������ʹ�����w������������������^�V������ԓ�����п�����ҺpH=12�ɴ_��Mg2+���M�����������(j��)�ṩ�Ĕ�(sh��)��(j��)Ӌ��������˕r��ҺB��Mg2+���|(zh��)������Ȟ�_________________������