
┐Ų─┐Ż║ üĒį┤Ż║īŻĒŚŅ} Ņ}ą═Ż║īŹ“×Ņ}

▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║ üĒį┤Ż║īŻĒŚŅ} Ņ}ą═Ż║īŹ“×Ņ}
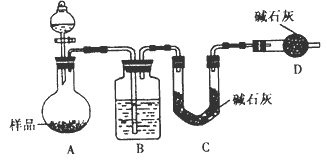
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║ üĒį┤Ż║īŻĒŚŅ} Ņ}ą═Ż║īŹ“×Ņ}
 COĪ³+H2O) įć╗ž┤Ž┬┴ąå¢Ņ}Ż║
COĪ³+H2O) įć╗ž┤Ž┬┴ąå¢Ņ}Ż║
 ( )Ī·( )Ī·( )Ī·╩š╝»ÜŌ¾w
( )Ī·( )Ī·( )Ī·╩š╝»ÜŌ¾w▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║ üĒį┤Ż║īŻĒŚŅ} Ņ}ą═Ż║īŹ“×Ņ}


▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║ üĒį┤Ż║īŻĒŚŅ} Ņ}ą═Ż║īŹ“×Ņ}
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║ üĒį┤Ż║īŻĒŚŅ} Ņ}ą═Ż║īŹ“×Ņ}
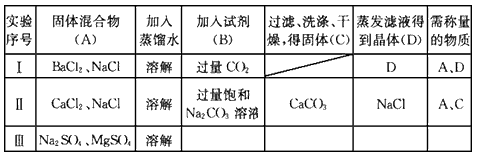
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║ üĒį┤Ż║īŻĒŚŅ} Ņ}ą═Ż║īŹ“×Ņ}
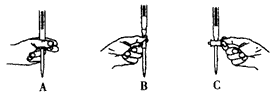
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║ üĒį┤Ż║īŻĒŚŅ} Ņ}ą═Ż║īŹ“×Ņ}
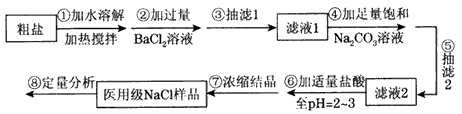
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║ üĒį┤Ż║▀|īÄ╩ĪŲ┌ųąŅ} Ņ}ą═Ż║īŹ“×Ņ}
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║ üĒį┤Ż║šŃĮŁ╩Īį┬┐╝Ņ} Ņ}ą═Ż║å╬▀xŅ}
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīW(xu©”)ąŻā×(y©Łu)▀x - ŠÜ┴Ģ(x©¬)āį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ō(li©ón)ŠW(w©Żng)▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW(w©Żng)╔Žėą║”ą┼Žó┼eł¾īŻģ^(q©▒) | ļŖą┼įp“_┼eł¾īŻģ^(q©▒) | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^(q©▒) | ╔µŲ¾ŪųÖÓ(qu©ón)┼eł¾īŻģ^(q©▒)
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com